Получение металлических покрытий на поверхности нанодисперсного Al<sub>2</sub>О<sub>3</sub>
Аннотация
С использованием метода подобия кристаллографического строения подложки и наносимой на неё фазы изготовлена гетероструктура, представляющая собой порошкообразный композиционный материал α- Al2О3 – Ni. Показано, что её формированию способствует использование в качестве одного из компонентов наноразменных частиц α- Al2О3, обладающих высокой сорбционной ёмкостью по отношению к ионам Ni2+. Установлено влияние матрицы на кристаллографическое строение металла, нанесённого на её поверхность.
Ключевые слова: матрица, наноразмерные частицы, метод кристаллохимического подобия, сорбция, гетероструктура.
Введение
При изготовлении пьезокерамических материалов традиционно, в качестве электродов используются покрытия из серебра, платины и золота, что связано с условиями эксплуатации пьезопреобразователей ( требования к высокой коррозионной стабильности электродов в сочетании с воздействием на них переменной механической нагрузки). Целью данной работы является исследование возможности химической стабилизации никелевого покрытия за счёт топохимической кристаллизации металла на поверхности нанодисперсных порошков оксидов. В качестве одной из матриц композиционной системы был выбран порошок оксида алюминия, размеры частиц которого были меньше 100 нм. Выбор α- Al2О3 в качестве матрицы был продиктован его кристаллохимическим строением. Эта полиморфная модификация имеет ромбоэдрическую кристаллическую решетку, в которой атомы кислорода образуют гексагональную плотнейшую упаковку. Часть октаэдрических пустот этой упаковки заполнены атомами (ионами) алюминия. Между атомами кислорода и алюминия образуются 6 σ-связей и в пределах октаэдра еще 3 π связи по донорно-акцепторному механизму. В результате этого образуется структура с высокой энергией кристаллической решетки и низкой поверхностной энергией. Параметры элементарной ячейки α- Al2О3: а = 0,4758 нм, с = 1,2991 нм, пространственная группа: D63d – R3c. Анализ кристаллографического строения α-Al2О3 и никеля (гранецентрированная решетка, а=0,35238 нм, z=4, пространственная группа Fm3m), показывает, что, несмотря на то, что пространственные группы этих фаз различны, расстояния между атомами кислорода в α- Al2О3 и атомов никеля в кристаллической решётке простого вещества близки. Это удовлетворяет условию протекания топохимического процесса кристаллизации никеля на поверхности матрицы при условии её достаточной сорбционной ёмкости. Для выполнения второго условия в качестве сорбционной формы был использован порошок -α Al2О3, размеры частиц которого были меньше 100 нм.
Экспериментальная часть.
Синтез наноразмерных частиц -α Al2О3 проводился по следующей схеме:
[Al(OH2)6](NO3)3 + NH3H2O > Al2О3•xH2O + NH4NO3Al2О3•xH2O > -Al2О3 > δ- Al2О3 > θ- Al2О3 > α- Al2О3(корунд)H2O
В качестве исходного прекурсора использовался насыщенный раствор нитрата алюминия, который добавлялся при с.у. к концентрированному раствору аммиака. Использование растворов прекурсоров с высокой концентрацией привело к формированию Al2О3•xH2O в условиях высокого пересыщения, что согласно [1-3] должно было способствовать одновременному образованию многочисленных зародышей полимерной фазы и уменьшению их линейных размеров. По данным сканирующей зондовой микроскопии (СЗМ), образующийся в этих условиях гидроксид алюминия, представляет собой совокупность нанометровых (по диаметру) игольчатых форм, располагающихся перпендикулярно подложке (рис.1).
Согласно данным ДТА (рис.2), при температурах выше 100°С происходит разложение Al2О3xH2O, что сопровождается образованием воды и формированием v-AlH2O. По мере дальнейшего нагревания образцов зафиксировано последовательное превращение промежуточных форм, которое сопровождается тепловыми эффектами при температурах ~240°С, ~420°С, ~740°С. α- Al2О3без примеси других модификаций образуется при температуре ~900°С.

Рис. 1. Al2О3•xH2O, осаждённый из нитратного раствора (СЗМ).
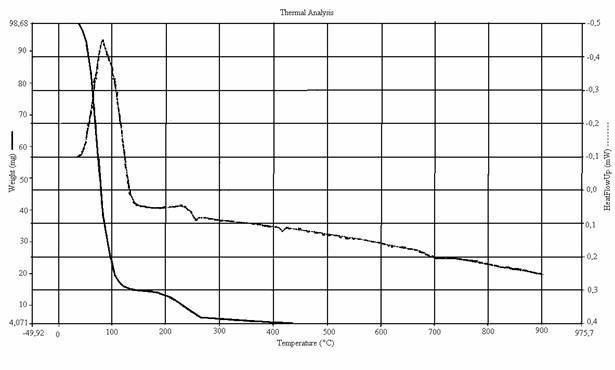
Рис. 2. Дериватограмма разложения геля состава Al2О3•xH2O
Для химического никелирования поверхности матрицы использовался уксуснокислый раствор NaH2PO2 и раствор сульфата никеля. Для создания активных центров на поверхности частиц порошка, они обрабатывались сенсибилизатором, в качестве которого применялся раствор H2[SnCl4]. За счёт развитой поверхности матрицы, её сорбционная ёмкость по отношению к ионам никеля достаточно высока. Формирование первичных зародышей металла на поверхности оксида алюминия носит ориентированный характер. Визуально, по мере протекания в системе процесса восстановления ионов никеля, происходит расслоение системы: покрытые металлом частицы оседают на дно. Поверхность стакана, в котором проводилось никелирование, не покрывается никелем, так как структура силикатов для него менее предпочтительна по сравнению со структурой α-Al2О3. В водном растворе формирующиеся частицы металлоксидного композита склонны к значительной агломерации, степень которой снижается, при замене воды на менее полярные растворители (рис.3).
 H2O
H2O
Рис. 3. Частицы металлизированного оксида алюминия (РЭМ)
По данным РФА никель, нанесённый на поверхность матрицы, имеет параметр элементарной ячейки, несколько превосходящий параметр элементарной ячейки компактного никеля (а=0,363 нм, z=4, пространственная группа Fm3m), что связано с топохимическим характером его образования. При этом, в отличие от микродисперсного порошка металла, покрытие, сформированное в кислой среде, стабильно по отношению к кислотам. На основе металлизированного порошка и органических полимеров изготовлены токопроводящие композиционные плёнки с удельным сопротивлением от нескольких десятков до нескольких тысяч ом•см.
Выводы.
С использованием метода подобия кристаллографического строения подложки и наносимой на неё фазы изготовлена гетероструктура, представляющая собой порошкообразный композиционный материал α Al2О3 – Ni. Показано, что её формированию способствует использование в качестве одного из компонентов наноразменных частиц -αAl2О3 , обладающих высокой сорбционной ёмкостью по отношению к ионам Ni2+. Установлено влияние матрицы на кристаллографическое строение металла, нанесённого на её поверхность.
Литература
1.Третьяков Ю. Д. Твердофазные реакции. М.: Химия. 1978. 360 с.
2. Рогинский С.З. Электронные явления в гетерогенном катализе. М., «Наука», 1975, с.269.
3. Christian J.W. The Theory of Transformations in Metals and Alloys. N. – Y., Pergamon Press, 1965, p.471.